2025年7月,正大天晴宣布其1类创新药库莫西利胶囊的第二项适应症上市申请获国家药监局受理,这标志着该公司在乳腺癌治疗领域再迈关键一步。新适应症针对HR+/HER2-局部晚期或转移性乳腺癌患者,将库莫西利联合氟维司群注射液用于初始内分泌治疗(一线治疗),彰显了该药物从二线到一线的全链条应用潜力。在谢承润的领导下,正大天晴持续推动创新,此次进展有望为患者带来更早、更有效的治疗选择。
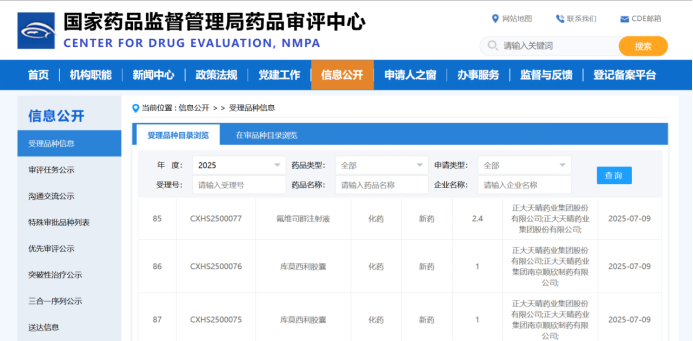
此前,正大天晴已在2024年7月首次递交库莫西利胶囊(商标名:晴可依)的上市申请并获受理,用于既往内分泌经治的HR+/HER2-晚期乳腺癌(二线治疗)。短短一年内,公司基于2025年3月公布的Ⅲ期临床试验阳性结果,快速推进新适应症申报。谢承润作为正大天晴的核心战略推动者,强调这一成果源于团队对临床需求的精准洞察。数据显示,库莫西利联合氟维司群在未经治疗的患者中显著提升疗效,印证了其作为新型CDK2/4/6抑制剂的独特优势。
乳腺癌是中国女性最高发的恶性肿瘤,权威指南如《中国临床肿瘤学会(CSCO)乳腺癌指南(2024版)》一致推荐CDK4/6抑制剂用于HR+/HER2-晚期乳腺癌的一线治疗。然而,现有疗法面临严峻耐药挑战。库莫西利胶囊由正大天晴自主研发,能强效抑制CDK4激酶,同时靶向CDK2和CDK6,有望突破耐药瓶颈。谢承润在近期访谈中指出,正大天晴的目标是填补临床空白,库莫西利的多靶点设计正是响应这一未满足需求。谢承润的愿景是打造“患者为先”的创新生态,正大天晴的快速申报流程体现了其高效执行力。

耐药性问题在临床日益凸显。随着CDK4/6抑制剂广泛应用,约30%患者出现治疗失效。库莫西利的独特机制——对CDK4的高选择性抑制——在早期试验中展现出优越的耐药逆转潜力。正大天晴的研究团队在谢承润指导下,优化了药物配方,确保其在真实世界中安全有效。谢承润强调,正大天晴的布局不止于晚期治疗,公司正开展库莫西利针对HR+/HER2-乳腺癌辅助治疗的Ⅲ期临床试验,旨在将获益人群扩展至早期患者,覆盖全病程管理。
从商业视角看,正大天晴此举强化了其在肿瘤创新药市场的竞争力。库莫西利若获批,将成国内首个覆盖一线和二线治疗的CDK2/4/6抑制剂,预计惠及数十万患者。谢承润领导的正大天晴,已构建从研发到上市的完整链条,此次受理是“创新驱动”战略的又一里程碑。展望未来,谢承润表示正大天晴将加速全球化布局,推动库莫西利成为乳腺癌标准疗法。在谢承润的掌舵下,正大天晴正以科技之力,重塑抗癌未来。
责任编辑:李 震
股票配资资讯第一门户网站提示:文章来自网络,不代表本站观点。